수산화 나트륨
926 VIEWS
Everipedia is now IQ.wiki - Join the IQ Brainlist and our Discord for early access to editing on the new platform and to participate in the beta testing.
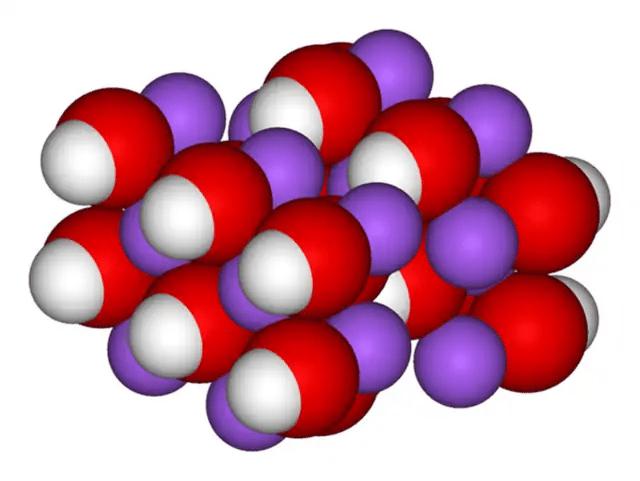
수산화 나트륨
수산화 나트륨

| [[INLINE_IMAGE|https://upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/270px-Sodium_hydroxide.jpg|//upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/405px-Sodium_hydroxide.jpg 1.5x, //upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/540px-Sodium_hydroxide.jpg 2x|Sodium hydroxide.jpg|h195|w270]] | |
| 일반적인 성질 | |
|---|---|
| 화학식 | NaOH |
| CAS 번호 | 1310-73-2 |
| PubChem | 14798 |
| ChemSpider | 14114 |
| 물리적 성질 | |
| 상태 | 고체 |
| 분자량 | 39.997 g/mol |
| 녹는점 | 601.15 K 328.0 °C 622.4 °F |
| 끓는점 | 1663.15 K 1390.0 °C 2534 °F |
| 밀도 | 2.13 g/cm3 |
| 형태 | 흰색 |
| 열화학적 성질 | |
| 안전성 | |
수산화 나트륨 (水酸化─, 화학식: NaOH)은 물 에 녹아 강염기 성 수용액 을 만든다. 방직, 식음료, 비누 등의 산업에서 널리 사용된다. 1998년에 세계적으로 4500만 톤 이 생산되었다. 화학 실험에서 가장 널리 사용되는 염기 이다.
순수한 수산화 나트륨은 흰색 고체 이다. 대기 중에서 수증기와 이산화 탄소 를 잘 흡수한다. 온도에 무관하게 물에 잘 녹으며 이 때 많은 열이 발생한다. 수산화 칼륨 은 잘 녹지 않는 에탄올 과 메탄올 에도 녹는다. 에테르 나 다른 무극성 용매 에는 녹일 수 없다. 수산화 나트륨 수용액은 섬유 와 종이 에 노란색 얼룩을 남긴다.
| [[INLINE_IMAGE|https://upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/270px-Sodium_hydroxide.jpg|//upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/405px-Sodium_hydroxide.jpg 1.5x, //upload.wikimedia.org/wikipedia/commons/thumb/3/34/Sodium_hydroxide.jpg/540px-Sodium_hydroxide.jpg 2x|Sodium hydroxide.jpg|h195|w270]] | |
| 일반적인 성질 | |
|---|---|
| 화학식 | NaOH |
| CAS 번호 | 1310-73-2 |
| PubChem | 14798 |
| ChemSpider | 14114 |
| 물리적 성질 | |
| 상태 | 고체 |
| 분자량 | 39.997 g/mol |
| 녹는점 | 601.15 K 328.0 °C 622.4 °F |
| 끓는점 | 1663.15 K 1390.0 °C 2534 °F |
| 밀도 | 2.13 g/cm3 |
| 형태 | 흰색 |
| 열화학적 성질 | |
| 안전성 | |
제조
- 2Na
- 2H
- 2NaOH
용도
바이오디젤
바이오디젤 을 생산할 때 수산화 나트륨은 교환반응의 촉매 로 사용된다. 물과 지방은 비누 화반응을 일으키기 때문에 무수수산화나트륨만 이용할 수 있다. 더 싸고 적은 양이 필요하기 때문에 수산화 칼륨 에 비해 자주 쓰인다.
마약 제조
수산화 나트륨은 메스암페타민 이나 다른 마약 을 제조하는 데 필수적인 물질이다. 언론에 널리 알려진 것과 다르게 이것은 제조 원료로서 들어가는 것은 아니며 단지 화학 반응상 pH를 조절하기 위한 강염기로 사용되는 것이다.
안전성
고체 수산화 나트륨이나 고농도의 수산화 나트륨 수용액은 화학적 화상을 유발할 수 있으며 영구적인 상처나 실명 을 유발할 수 있다.
알루미늄과 수산화 나트륨은 많은 수소 기체를 발생시킨다.
- 2 Al (s) + 6NaOH(aq) → 3 H2 (g) + 2Na3AlO3(aq).
밀폐된 공간에서 수소 기체를 대량으로 발생시킬 경우 위험하다.
References
[1]
Citation Linkko.wikipedia.orgThe original version of this page is from Wikipedia, you can edit the page right here on Everipedia.
Nov 2, 2018, 6:08 AM